
Mieux respirer grâce à un diagnostic précoce d’asthme ou de MPOC
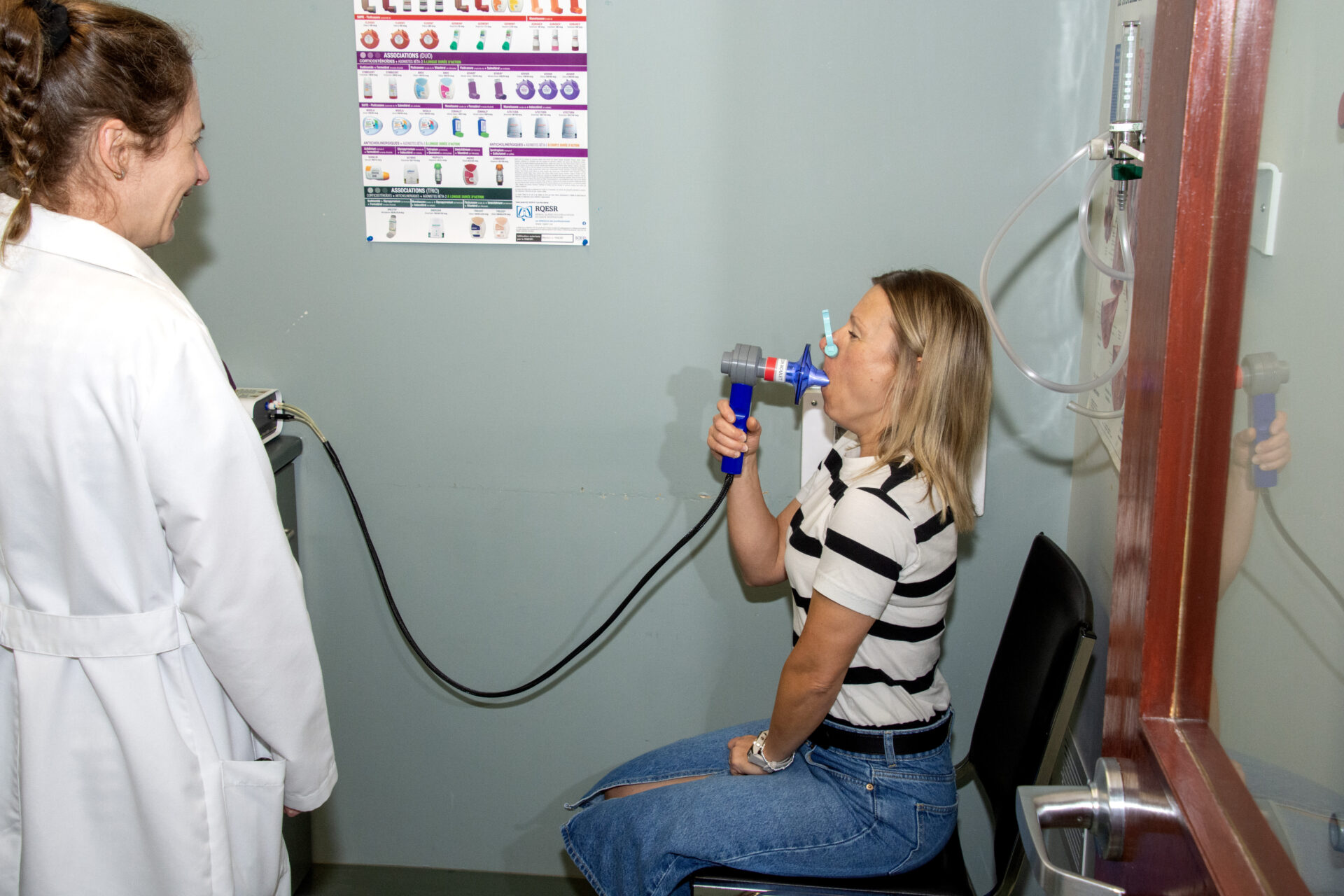
Chaque jour, des milliers de Canadiens vivent avec des symptômes respiratoires comme la toux, l’essoufflement ou des sifflements, sans savoir qu’ils pourraient souffrir d’asthme ou de maladie pulmonaire obstructive chronique (MPOC). Ces maladies, lorsqu’elles ne sont pas diagnostiquées à temps, peuvent entraîner une détérioration progressive de la santé respiratoire et une diminution importante de la qualité de vie. Il est désormais bien établi que plus une maladie respiratoire est identifiée précocement, plus les interventions thérapeutiques sont susceptibles d’en freiner la progression et d’en atténuer les conséquences sur la qualité de vie.
C’est dans ce contexte qu’a été menée l’étude UCAP (Uncovering Chronic Obstructive Pulmonary Disease and Asthma through Primary Care), une initiative de recherche d’envergure nationale à laquelle les docteurs LouisPhilippe Boulet et Andréanne Côté ont fièrement contribué. Publiée dans la prestigieuse revue New England Journal of Medicine, cette étude marque une avancée majeure dans la détection précoce des maladies respiratoires chroniques.

Une étude d’envergure nationale
Entre 2017 et 2024, les équipes de recherche de l’étude UCAP ont contacté plus d’un million de foyers à travers le Canada afin d’identifier des adultes présentant des symptômes respiratoires persistants, mais n’ayant jamais reçu de diagnostic de maladie respiratoire. Au total, 508 participants ont été recrutés, dont plus d’une centaine par l’équipe du Dr Louis-Philippe Boulet et de la Dre Andréanne Côté.
Les participants chez qui un diagnostic d’asthme ou de MPOC a été posé ont été répartis en deux groupes. Le premier groupe a été pris en charge par une équipe multidisciplinaire comprenant un pneumologue et une éducatrice spécialisée. Ces usagers ont reçu un enseignement personnalisé sur la gestion de leur maladie, incluant l’utilisation adéquate des inhalateurs, l’importance de l’exercice physique, l’arrêt du tabac et l’adhésion au traitement médicamenteux. Le second groupe a poursuivi les soins habituels avec leur médecin de famille.
Des résultats probants
Les résultats de l’étude sont sans équivoque. Une fois un diagnostique posé, le suivi par le médecin de famille a permis une amélioration notable de l’état de santé des usagers. Toutefois, les bénéfices ont été encore plus marqués chez ceux qui ont bénéficié d’un suivi spécialisé. Ces usagers ont eu significativement moins de consultations médicales et d’hospitalisations liées à des problèmes respiratoires. Ils ont également rapporté une réduction importante de leurs symptômes, notamment la toux, l’essoufflement et les sifflements. Leur qualité de vie s’est améliorée, comme en témoignent les résultats de questionnaires validés, et leur fonction pulmonaire s’est améliorée, ce qui a été confirmé par des tests respiratoires. Ces constats soulignent l’importance cruciale d’un diagnostic précoce et d’une prise en charge multidisciplinaire pour les personnes atteintes de maladies respiratoires chroniques, générant des bénéfices substantiels tant pour les usagers que pour l’ensemble du système de santé.
Une contribution significative
La participation des équipes de recherche des docteurs Boulet et Côté à cette étude a été essentielle. Grâce à l’expertise d’équipes cliniques et de recherche, elles ont pu recruter un nombre important de participants et assurer un suivi rigoureux. Cette contribution a permis de démontrer concrètement l’impact positif d’une approche multidisciplinaire dans la gestion des maladies respiratoires.
L’étude UCAP illustre également le rôle central que joue le Centre de recherche de l’Institut dans l’avancement des connaissances en santé respiratoire, tant au niveau provincial que national. Elle témoigne de notre engagement à améliorer la qualité de vie des usagers par la recherche, l’innovation et l’excellence clinique.



Sur la photo de groupe, de gauche à droite :
Johanne Lepage, Marie-Eve Boulay, Dre Andréanne Côté et Dr Louis-Philippe Boulet

Les médicaments de la classe des agonistes du récepteur du GLP-1 (GLP-1RA), comme l’Ozempic ou le Wegovy, ont révolutionné la prise en charge de l’obésité. Initialement développés pour traiter le diabète de type 2, leur capacité remarquable à induire une perte de poids importante a suscité un intérêt clinique et scientifique mondial. Pourtant, malgré leur efficacité, les mécanismes neuronaux précis par lesquels ces molécules réduisent l’appétit demeuraient jusqu’à récemment mal compris.
L’équipe du Dr Alexandre Caron a récemment levé le voile sur une pièce manquante de ce casse-tête pharmacologique. Dans une étude parue en 2024 dans la revue Neuroendocrinology, l’équipe a identifié une nouvelle population de neurones dans le cerveau qui pourrait jouer un rôle central dans l’effet coupe-faim des GLP-1RA.
Ces neurones, localisés dans le noyau arqué de l’hypothalamus, une région clé pour le contrôle de l’appétit, expriment une protéine peu connue appelée Cellular Retinoic Acid Binding Protein 1 (CRABP1). Les travaux de l’équipe du Dr Caron ont démontré que les neurones exprimant CRABP1 constituent une nouvelle famille de neurones GABAergiques, distincte des deux populations hypothalamiques bien connues : les neurones produisant la proopiomelanocortin (POMC – suppressifs de l’appétit) et les neurones exprimant l’Agouti-Related Peptide (AgRP — stimulateurs de l’appétit).
Grâce à des techniques de cartographie cérébrale, d’hybridation in situ et d’immunohistochimie, l’équipe a caractérisé cette nouvelle population et démontré une forte expression de récepteurs pour plusieurs hormones métaboliques, dont la leptine et le GLP-1. Cela suggérait d’emblée un rôle potentiel dans la régulation de l’appétit.
Pour tester cette hypothèse, l’équipe du Dr Caron a évalué l’activation de ces neurones chez la souris en réponse à différentes conditions métaboliques. Les résultats ont démontré que les neurones CRABP1 sont particulièrement actifs en situation de jeûne et que leur activité diminue après un repas ou après l’administration du liraglutide, un médicament de la même famille que l’Ozempic. En d’autres mots, le liraglutide semble « duper » ces neurones en leur faisant croire qu’un repas a été consommé, ce qui pourrait contribuer à déclencher la sensation de satiété.
Ces résultats sont d’autant plus intéressants qu’ils pourraient expliquer pourquoi les analogues du GLP-1, comme le sémaglutide (la molécule active de l’Ozempic), ont un effet anorexigène si puissant. En identifiant une cible neuronale précise impliquée dans ce mécanisme, les travaux de l’équipe du Dr Caron ouvrent la voie au développement de nouveaux médicaments potentiellement plus spécifiques, plus efficaces ou avec moins d’effets secondaires.
L’identification des neurones CRABP1 représente également une avancée fondamentale dans la compréhension du cerveau dans l’obésité. Pendant des décennies, les recherches sur le contrôle central de l’appétit se sont concentrées sur les neurones POMC et AgRP. Toutefois, des études récentes ont montré que l’inhibition de neurones GABAergiques peut complètement renverser l’obésité chez des souris génétiquement obèses, indiquant l’existence de souspopulations GABAergiques encore non identifiées jouant un rôle déterminant dans l’équilibre énergétique. Les travaux de l’équipe du Dr Caron viennent justement combler cette lacune.
D’un point de vue translationnel, cette découverte a des implications majeures. L’obésité est une maladie multifactorielle complexe et les traitements pharmacologiques actuels ne fonctionnent pas de manière égale pour tous. Comprendre les circuits neuronaux impliqués dans la régulation de l’appétit permet non seulement de mieux prédire qui répondra à un traitement, mais aussi de concevoir des approches plus personnalisées. Par ailleurs, le fait que ces neurones soient sensibles à la fois à la leptine et au GLP-1 laisse entrevoir une possible convergence de plusieurs signaux métaboliques sur cette population, ce qui pourrait devenir une cible de choix pour les combinaisons thérapeutiques de demain. En somme, les travaux de l’équipe du Dr Alexandre Caron contribuent à déchiffrer les bases neuronales de l’effet coupe-faim des GLP-1RA, tout en mettant en lumière une nouvelle composante du réseau hypothalamique de régulation de l’équilibre énergétique. Dans un contexte où l’obésité représente un défi de santé publique majeur, chaque avancée dans la compréhension fine des mécanismes impliqués nous rapproche d’une prévention plus efficace, de traitements plus adaptés et d’un avenir où la gestion de cette maladie sera davantage fondée sur les circuits cérébraux qui la sous-tendent.



Sur la photo de groupe, de gauche à droite :
Luce-Marie Loumou, Laura Tribouillard, Bernie Efole, Fatima Hjeij, Sarra Beji, Mylène Bastien, Soumia Fenni, Audrey Turmel et Dr Alexandre Caron

La maladie cardiovasculaire demeure la principale cause de morbidité et de mortalité au Québec et au Canada. La dernière décennie a été marquée par une progression préoccupante de la prévalence de la maladie cardiovasculaire chez les personnes âgées de 30 à 50 ans. Neuf personnes sur 10 de plus de 20 ans présentent au moins un facteur de risque de maladie cardiovasculaire. Près de 80 % des maladies cardiovasculaires sont évitables, ce qui souligne l’importance cruciale des activités de dépistage et de prévention. Certaines populations au Québec, notamment celles issues de milieux défavorisés, de l’immigration, les peuples autochtones ou encore les populations vivant en régions éloignées, rencontrent des obstacles significatifs à l’accès aux avancées récentes en matière de prévention et de soins spécialisés et elles sont souvent confrontés à des résultats de santé moins favorables, particulièrement les femmes. Ces disparités en santé témoignent des nombreux facteurs contextuels, environnementaux, socioculturels et individuels qui influencent l’apparition et l’évolution des maladies, l’accès aux soins et l’efficacité des interventions.
Les peuples autochtones sont confrontés à des défis en santé plus importants en raison de facteurs inhérents complexes comme les traumatismes intergénérationnels, les obstacles à l’autodétermination, les préjugés et la discrimination dans les soins de santé. L’effet fondateur, bien documenté au Québec, notamment dans les régions de Charlevoix, du Saguenay et de la Côte-Nord, est lié à une prédisposition génétique marquée aux maladies cardiovasculaires ainsi qu’à une incidence accrue d’événements cardiovasculaires précoces avant l’âge de 55 ans. Cette situation unique au Québec souligne la nécessité de dépistages et d’interventions ciblées auprès de ces populations à haut risque. De plus, la sous-représentation de ces populations en recherche nuit à l’avancée des soins qui leur sont offerts. En effet, le manque de données probantes limite notre capacité à développer des stratégies de dépistage, de prévention et de soins adaptés à leurs besoins et perpétue les inégalités en matière de santé.
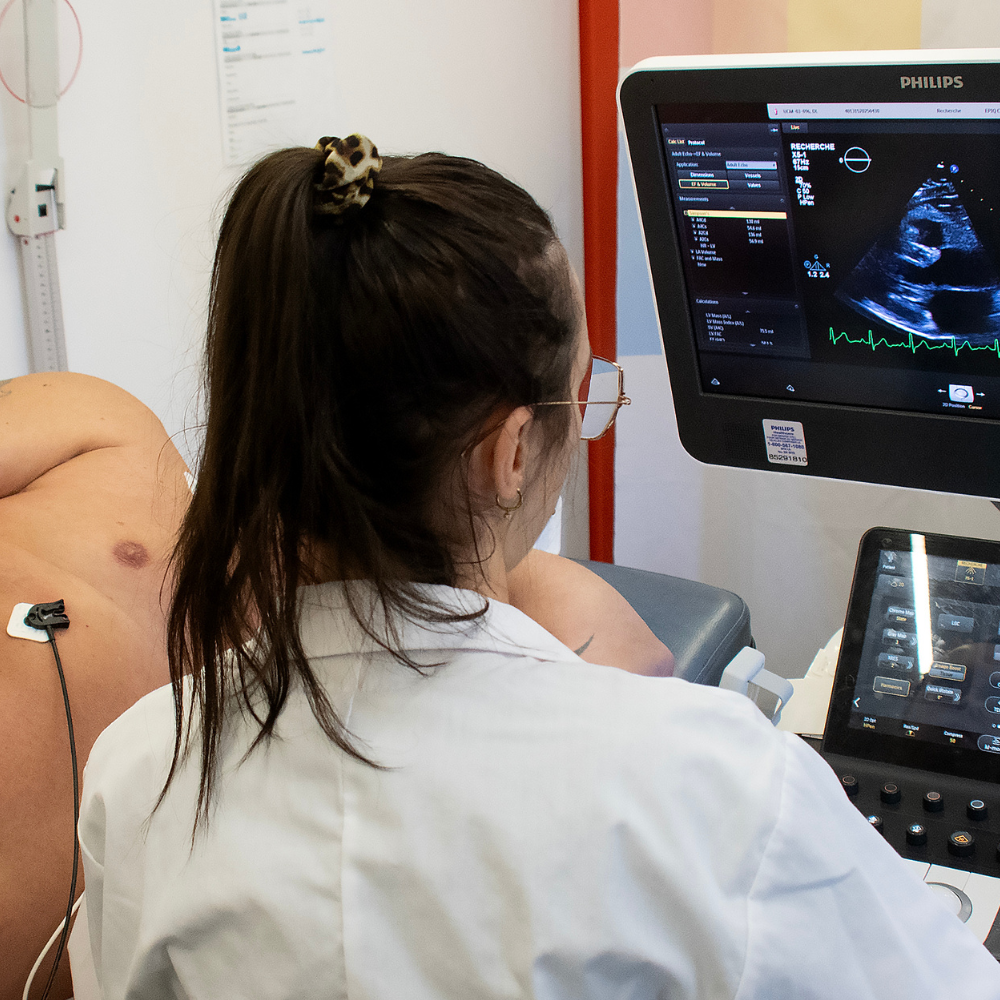
Pour pallier les importantes inégalités en santé et d’accès aux soins spécialisés, la Dre Marie-Ève Piché et son équipe ont mis en place une unité clinique mobile déployée dans les communautés sous-représentées, incluant les communautés autochtones et éloignées, qui vise notamment à : 1) identifier les obstacles et facilitateurs à l’engagement des populations sous-représentées dans la recherche et les soins; 2) évaluer les facteurs de risque cardiovasculaire et la prévalence des maladies métaboliques et cardiovasculaires chez les populations sous-représentées à l’aide de technologies émergentes et des approches novatrices et 3) mesurer l’impact de cette approche préventive communautaire sur la santé cardiovasculaire des populations ciblées. Cette initiative permet également de mieux comprendre les formes précoces de maladies cardiovasculaires qui touchent particulièrement les populations en régions éloignées et les communautés autochtones du Québec. En ouvrant ses portes directement dans les communautés, l’unité clinique mobile propose des activités de recherche à fort impact, qui répondent de manière dynamique aux besoins évolutifs de chaque communauté. Les retombées pour ces communautés isolées sont importantes et les actions d’évaluation et de prévention permettent d’éviter des comorbidités et de prévenir en amont des événements cardiaques.
Un projet de faisabilité a été initié en 2024 par l’équipe de la Dre Piché en collaboration avec cinq groupes sous-représentés, dont trois communautés autochtones. Cette initiative a permis d’obtenir des données préliminaires uniques en santé. Grâce à la collaboration avec les membres des communautés sous-représentés et à une subvention récente obtenue des Instituts de recherche en santé du Canada qui met l’accent sur l’équité et l’inclusivité, cette initiative en santé sera étendue afin de tester le modèle dans diverses communautés et régions éloignées au cours d’une période de cinq ans. Des technologies émergentes et des approches novatrices (p. ex., imageries cardiaque et vasculaire avancées, outils de surveillance à distance, intelligence artificielle et plateformes numériques) seront mises en œuvre pour renforcer la surveillance ainsi que le diagnostic et améliorer l’accessibilité de même que l’engagement des populations sousreprésentées, notamment les populations géographiquement isolées. Axée sur l’équité et l’inclusivité, cette initiative en santé vise à produire des données novatrices et pertinentes sur les facilitateurs et les obstacles à l’accès aux soins dans ces populations touchées de manière disproportionnée par les maladies cardiovasculaires, incluant les communautés autochtones pour lequel l’Institut assure un leadership provincial et national. Cette initiative permettra de créer des possibilités de développement des capacités locales et de mobilisation des connaissances auprès de ces dernières. Ces recherches contribueront au codéveloppement d’interventions préventives adaptées avec les communautés ciblées afin de codévelopper des interventions adaptées à leurs besoins et à leurs réalités, tout en assurant un cadre culturellement sécurisant. Enfin, ces travaux permettront également d’améliorer la prévention de conditions cardiovasculaires tôt dans la vie, particulièrement au sein de populations touchées de manière disproportionnée par les maladies cardiovasculaires.


Sur la photo de groupe, de gauche à droite :
Lavinia El Khoury, Maëlle Blais, Julie Desjardins, Dre Marie-Eve Piché, Raven Larocque Laliberté, Dre Caroline Samhani et Catherine Pichette.
Absentes sur la photo : Johanne Marin, Laurie Bilodeau, Anne-Marie Doucet, Marie Rousseau-Demers et Alexandra Larochelle
*Données tirées de notre rapport annuel 2024-2025




